人工智慧睡眠眼罩iSleep Better改善失眠

作者
吳漢忠簡介
中研院特聘研究員兼生醫轉譯研究中心主任,擁有96項專利及逾110篇論文發表,榮獲美國發明家學院院士等25項獎項。
單位
中央研究院文章來源
https://cancerres.aacrjournals.org/content/80/22/5035.short
https://www.sciencedirect.com/science/article/pii/S0304383518304488-
標籤
-
分享文章
基於國際授權條款4.0,您可免費分享此篇文章
中央研究院細胞與個體生物研究所特聘研究員暨生醫轉譯研究中心主任吳漢忠的研究團隊發表了一項研究成果,解開EpCAM如何促進癌細胞生長,以及如何中止這項機制之謎。EpCAM會大量表現於惡性腫瘤中,並且促進腫瘤惡化,所以用EpCAM作為打擊標的之癌症標靶療法極具開發價值。研究團隊研發的中和性單株抗體EpAb2-6,可抑制EpCAM訊息傳遞,並可直接引起細胞凋亡而殺死癌細胞,降低癌細胞中PD-L1蛋白的穩定,進而活化T細胞殺死癌細胞的能力。在動物實驗使用EpAb2-6和PD-L1抗體Atezolizumab的「聯合療法」,可有效抑制腫瘤生長。這些發現對未來臨床上治療EpCAM過量表現的癌症,提供了結合免疫療法的新策略。
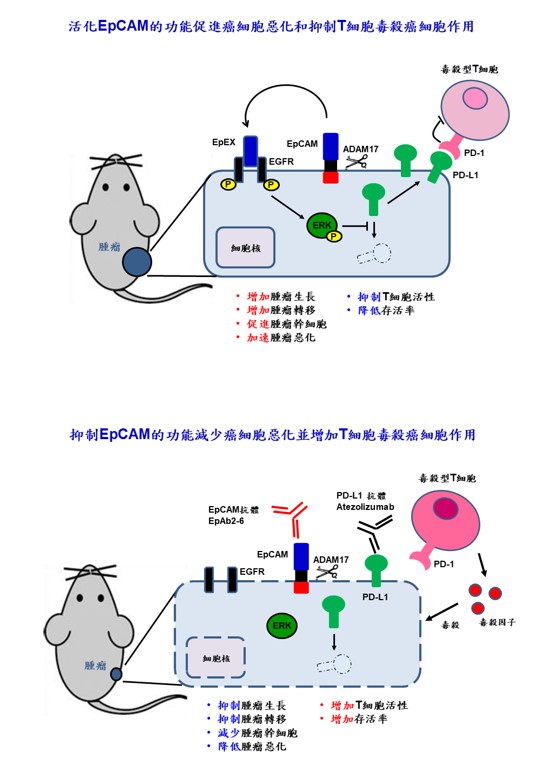
圖一:EpCAM的功能說明
癌症免疫療法可望更精準!在癌症研究中,上皮細胞黏附分子(EpCAM)被廣泛認為是辨認癌細胞的重要標的。近期,中央研究院細胞與個體生物研究所特聘研究員兼任生醫轉譯研究中心主任吳漢忠的研究團隊發表了一項研究成果,解開EpCAM如何促進癌細胞生長,以及如何中止這項機制之謎。團隊研發的新抗體EpAb2-6對癌症的診斷、標靶治療及造影都深具發展潛力,近期已刊登在國際期刊《癌症研究》(Cancer Research)。
EpCAM是一種在細胞膜上的蛋白質,常見於上皮組織和大量表現於惡性腫瘤中,與細胞黏附、遷移、增殖及腫瘤發生與惡化有關。研究團隊發現,它會透過訊息傳遞來穩定PD-L1的蛋白;而PD-L1正是使腫瘤細胞得以逃脫身體免疫系統監控,導致癌症惡化的蛋白質!目前,已證實只要抑制免疫檢查點蛋白(例如 PD-1 或CTLA-4)就能有效治療癌症,這也是2018年獲得諾貝爾生理醫學獎肯定並在醫學界備受重視的「癌症免疫療法」。
為了能精準辨識出癌細胞膜上的EpCAM,研究團隊研發出相對應的中和性單株抗體EpAb2-6,可抑制EpCAM的訊息傳遞功能,降低癌細胞中PD-L1蛋白的表現,進而導致腫瘤細胞死亡及活化T細胞殺死癌細胞的能力(圖一)。在大腸癌的動物實驗中,EpAb2-6展現了絕佳的腫瘤抑制能力及大幅提升小鼠的存活率。此外,在肺癌的動物實驗同時使用EpAb2-6 和PD-L1抗體Atezolizumab的「聯合療法」,可有效抑制腫瘤的生長。這些發現不僅更深入剖析EpCAM促使癌症惡化的分子機制,對未來臨床上治療EpCAM過量表現的癌症,也提供了結合免疫療法的新策略。
EpAb2-6抗體是目前唯一一株結合至細胞表面EpCAM後,直接誘發癌細胞死亡、抑制腫瘤幹細胞生長之單株抗體。作用機制不同於過去臨床試驗以ADCC/CDC為主之anti-EpCAM抗體(MT201與ING-1)。從動物模式證明,此抗體治療能延長小鼠存活率。EpAb2-6抗體功能、抗體互補性決定區序列(CDR)與其所辨認之抗原決定位(epitope)具進步性與新穎性,已獲得美國、日本、歐盟、中國與台灣專利保護。該抗體具高結合能力,在治療性抗體新藥開發上,極具優勢。更重要的是,85%腫瘤組織有大量EpCAM表現,未來更有機會應用於各種癌症治療。目前治療性抗體的市場中,尚未有anti-EpCAM抗體新藥,是該抗體之利基。
經實驗證實,這種中和性抗體EpAb2-6能與多種癌細胞的EpCAM結合,也能有效抑制腫瘤的生長和轉移,延長小鼠壽命。目前,此中和性抗體EpAb2-6在癌症的診斷、標靶治療及造影的應用,深具發展潛力,已取得世界多國的專利,並獲科技部價創計畫5,000萬元的支持,成立新創公司進駐國家生技研究園區,未來可望化研為用,造福人群。
訂閱電子報以獲得最新資訊
填寫連絡資訊以取得每月發行之電子報